Da Wikipedia, l'enciclopedia libera.
La
tavola periodica degli elementi (o semplicemente
tavola periodica) è lo schema con il quale vengono ordinati gli
elementi chimici sulla base del loro
numero atomico Z.
In onore del chimico russo, la tavola periodica degli elementi è anche detta tavola periodica di Mendeleev.
La tavola periodica [modifica]
La tavola periodica si articola in gruppi e periodi:
- ogni gruppo (colonna della tabella) comprende gli elementi che hanno la stessa configurazione elettronica esterna (modo in cui gli elettroni si dispongono attorno al nucleo). All'interno di ogni gruppo si trovano elementi con caratteristiche chimiche simili;
- ogni periodo (riga della tabella) inizia con un elemento il cui atomo ha come configurazione elettronica esterna un elettrone di tipo ns dove n è il numero quantico principale, e procedendo verso gli atomi successivi del periodo, il numero atomico Z aumenta di una unità ad ogni passaggio.[3]
Legenda per i colori dei numeri atomici:
- gli elementi numerati in blu sono liquidi a T = 298 K e p = 1 bar;
- quelli in verde sono gas a T = 298 K e p = 1 bar;
- quelli in nero sono solidi a T = 298 K e p = 1 bar;
- quelli in rosso sono artificiali e non sono naturalmente presenti sulla Terra (sono tutti solidi a T = 298 K e p = 1 bar). Il tecnezio è presente in minime quantità nelle miniere di uranio e nelle giganti rosse.
Organizzazione [modifica]
Nella moderna tavola periodica, gli elementi sono posti progressivamente in ciascun periodo da sinistra a destra secondo la sequenza dei loro numeri atomici, iniziando una nuova riga dopo un gas nobile. Il primo elemento nella riga successiva è sempre un metallo alcalino con un numero atomico più grande di un'unità rispetto a quello del gas nobile (ad es. dopo il
kripton, un gas nobile con il numero atomico 36, inizia una nuova riga con il
rubidio, un metallo alcalino con il numero atomico 37). Attualmente non esistono lacune perché tutti gli elementi tra l'
idrogeno e l'
ununoctio (elemento 118) sono stati scoperti. Poiché gli elementi sono collocati in sequenza secondo il numero atomico, le serie degli elementi sono a volte specificate da termini come "fino a" (ad es. fino al
ferro), "oltre" (ad es. oltre l'
uranio), o "da ... fino a" (ad es. dal
lantanio fino al
lutezio). A volte si usano informalmente anche i termini "leggero" e "pesante" per indicare i numeri atomici relativi (non le
densità), come nelle espressioni "più leggero del
carbonio" o "più pesante del
piombo", sebbene tecnicamente il peso o massa degli atomi degli elementi (i loro pesi atomici o masse atomiche) non sempre aumenti
in maniera monotona con i loro numeri atomici. A titolo di esempio il
tellurio, elemento 52, è in media più pesante dello
iodio, elemento 53.
[3]
L'idrogeno e l'
elio sono spesso collocati in posti diversi da quelli che indicherebbero le loro configurazioni elettroniche: l'idrogeno di solito è collocato sopra il
litio, in accordo con la sua configurazione elettronica, ma a volte è posto sopra il
fluoro,
[4] o perfino sopra il carbonio,
[4] in quanto si comporta in modo simile ad essi. L'elio è posto quasi sempre sopra il
neon, poiché sono chimicamente molto simili.
[5]
Il significato dei numeri atomici per l'organizzazione della tavola periodica non fu apprezzato finché non divennero chiare l'esistenza e le proprietà dei protoni e dei neutroni. Come ricordato in precedenza, le tavole periodiche di Mendeleev usavano invece i pesi atomici, informazioni determinabili ai suoi tempi con precisione accettabile, che funzionarono abbastanza bene nella maggior parte dei casi per offrire una presentazione di grande potenza predittiva, di gran lunga migliore di qualsiasi altra rappresentazione completa delle proprietà degli elementi chimici allora possibile. La sostituzione dei numeri atomici, una volta compresa, diede una sequenza definitiva per gli elementi, basata su numeri interi, utilizzata ancora oggi anche quando si stanno producendo e studiando nuovi elementi sintetici.
[6]
Metodi di raggruppamento [modifica]
Un
gruppo o
famiglia è una colonna verticale nella tavola periodica. I gruppi sono considerati il più importante metodo di classificazione degli elementi. In alcuni gruppi, gli elementi hanno proprietà molto simili e mostrano un chiaro andamento delle proprietà lungo il gruppo. In base al sistema di denominazione internazionale, i gruppi sono indicati numericamente da 1 a 18 dalla colonna più a sinistra (i metalli alcalini) alla colonna più a destra (i gas nobili).
[7] I sistemi di denominazione più vecchi differivano leggermente tra l'Europa e l'America.
[8]
Le moderne teorie quanto-meccaniche della struttura atomica spiegano le tendenze dei gruppi proponendo che gli elementi all'interno dello stesso gruppo hanno generalmente le stesse configurazioni elettroniche nel loro
guscio di valenza, che è il fattore più importante nella spiegazione delle loro proprietà simili.
[9]
Gli elementi dello stesso gruppo mostrano schemi di comportamento nel
raggio atomico, nell'
energia di ionizzazione e nell'
elettronegatività. Dall'alto in basso in un gruppo, i raggi atomici degli elementi aumentano. Poiché ci sono livelli di energia maggiormente riempiti, gli elettroni di valenza si trovano a maggiore distanza dal nucleo. Dall'alto, ogni elemento successivo ha una minore energia di ionizzazione perché è più facile allontanare un elettrone, in quanto gli elettroni sono meno strettamente legati. Similmente, un gruppo presenta una diminuzione dall'alto verso il basso dell'elettronegatività, dovuta a una distanza crescente tra gli elettroni di valenza e il nucleo.
[10]
Un
periodo o
serie è una riga orizzonatale nella tavola periodica. Sebbene i gruppi siano il modo più comune di classificare gli elementi, ci sono regioni in cui gli andamenti in senso orizzontale dei gruppi sono più significativi di quelli in senso verticale, come nel caso del blocco f, dove i
lantanidi e gli
attinidi formano due sostanziali serie di elementi di tipo orizzontale.
[11]
Gli elementi nello stesso periodo mostrano andamenti nel raggio atomico, nell'energia di ionizzazione, nell'
affinità elettronica e nell'elettronegatività. Muovendosi da sinistra a destra attraverso un periodo, il raggio atomico solitamente diminuisce. Ciò accade perché ciascun elemento successivo ha un protone e un elettrone aggiunto che fa sì che l'elettrone sia attirato più vicino al nucleo.
[12] Questa diminuzione del raggio atomico fa anche sì che l'energia di ionizzazione aumenti quando ci muove da sinistra a destra attraverso un periodo. Più strettamente legato è un elemento, maggiore è l'energia richiesta per allontanare un elettrone. L'elettronegatività aumenta allo stesso modo dell'energia di ionizzazione a causa dell'attrazione esercitata sugli elettroni dal nucleo.
[10] Anche l'affinità elettronica mostra una lieve tendenza da un lato all'altro di un periodo. I metalli (lato sinistro di un periodo) hanno generalmente una minore affinità elettronica dei non metalli (lato destro di un periodo), ad eccezione dei gas nobili.
[13]

Un diagramma della tavola periodica, che mette in evidenza i diversi blocchi.
A causa dell'importanza del guscio elettronico più esterno, le diverse regioni della tavola periodica sono talvolta chiamate
blocchi della tavola periodica, denominati secondo il sottoguscio in cui risiede l' "ultimo" elettrone.
[5] Il
blocco s comprende i primi due gruppi (metalli alcalini e metalli alcalino-terrosi) nonché l'idrogeno e l'elio. Il
blocco p comprende gli ultimi sei gruppi, che corrispondono ai gruppi da 13 a 18 nella numerazione IUPAC (da 3A a 8A in quella statunitense), e contiene, tra gli altri, tutti i
metalloidi. Il
blocco d comprende i gruppi da 3 a 12 secondo la numerazione IUPAC (o da 3B a 2B in quella statunitense) e contiene tutti i
metalli di transizione. il
blocco f, di solito collocato sotto il resto della tavola periodica, comprende i lantanidi e gli attinidi.
[14]
L'invenzione della tavola periodica [modifica]
| Proprietà periodiche |
Le proprietà caratteristiche di ciascun elemento che si è riscontrato periodicizzarsi lungo la tavola periodica sono, principalmente, queste:
|

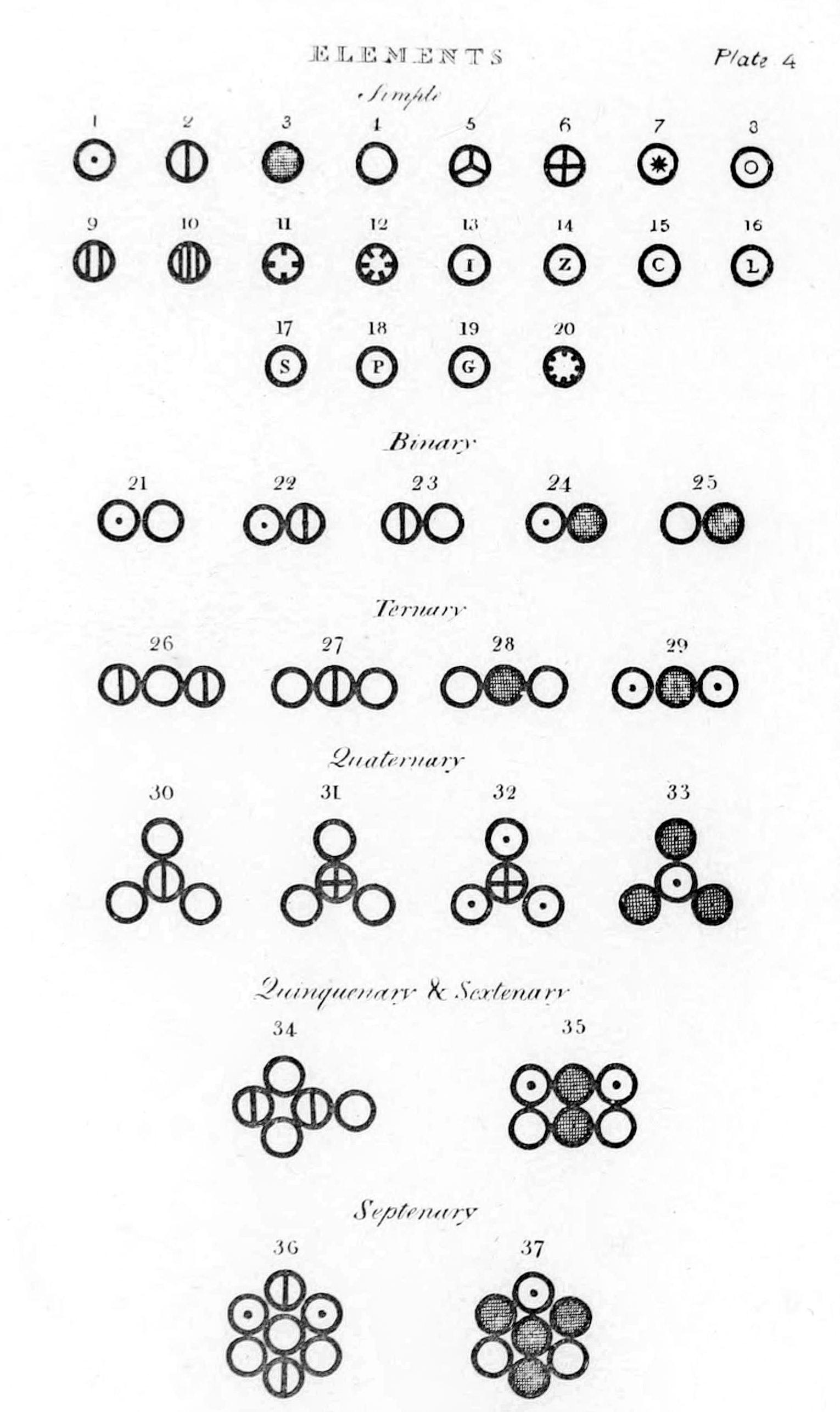
Una rappresentazione degli elementi di
John Dalton ("
A New System of Chemical Philosophy",
1808).
La necessità di ordinare le conoscenze che (grazie a ricerche empiriche) venivano accumulandosi sulle diverse sostanze venne sentita fin dai primordi della
chimica, e
Lavoisier propose (nel
1789) una prima forma di sistematica chimica. Bisogna, però, aspettare all'incirca il
1870 affinché si giunga al modello che, con le opportune aggiunte, è utilizzato ai giorni nostri.
Se gli elementi vengono disposti in ordine crescente di
numero atomico, inserendo in seguito altre proprietà, si può notare una ondulazione o una
periodicità di queste proprietà in funzione del numero atomico dell'elemento stesso. Il primo che riconobbe queste ricorrenze fu il chimico
tedesco Johann Wolfgang Döbereiner, che nel
1829per primo notò una certa quantità di
triadi, gruppi di tre elementi con queste similarità.
A questa intuizione fece seguito l'
inglese John Newlands, che sottolineò (nel
1865) come gli elementi di tipo simile fossero ricorrenti ad intervalli regolari di 8 posizioni, che lui assimilò alle
ottave musicali, anche se questa sua cosiddetta
legge delle ottave venne messa in ridicolo dai suoi contemporanei.
[15]
Fu proprio in quel periodo che
Meyer e
Mendeleev (indipendentemente l'uno dall'altro) assunsero il
peso atomicocome parametro per la classificazione periodica degli elementi, il che costituì un passo decisivo verso il più raffinato concetto di
numero atomico (del quale, nella chimica odierna, le proprietà fisico-chimiche degli elementi sono considerate funzioni periodiche). Meyer pubblicò i propri risultati qualche mese dopo Mendeleev, ed è per questo che molto spesso ci si riferisce alla tavola periodica degli elementi col solo nome di quest'ultimo. Egli ipotizzò anche che esistessero altri elementi, al momento non conosciuti, che occupavano le celle vuote della tabella; teoria che trovò conferme con la scoperta della struttura elettronica degli elementi tra la fine del
XIX e gli inizi del
XX secolo.
La ragione della particolare periodicità per serie di lunghezza diversa (2, 8, 8, 18, 18, 32, 32) è stata scoperta solo in seguito (ad opera principalmente di
Niels Bohr), ed è da ricercarsi nella tendenza al massimo riempimento possibile degli
orbitali atomici da parte degli
elettroni, che ha valore diverso a seconda del tipo di orbitale interessato, e al modo in cui si susseguono i diversi tipi orbitali per numeri atomici crescenti; si hanno infatti al massimo due elettroni per orbitale di tipo
s, al più sei elettroni per orbitali di tipo
p, al più dieci per orbitali
d, ed al più quattordici per orbitali tipo
f; inoltre gli orbitali si possono susseguire solo nell'ordine:
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p 8s (secondo la
regola di Aufbau).
[18]
A diversi gradi di riempimento dell'orbitale più esterno corrisponde una diversa reattività dell'intero atomo, per cui ad orbitali "completi" corrisponde la configurazione energetica più stabile (e quindi una reattività nulla), e ad orbitale esterno parzialmente "completo" corrispondono reattività via via maggiori quanto più il numero di elettroni si allontana da quello di una configurazione stabile; questa diversa reattività a livello macroscopico determina molte delle proprietà chimiche dell'elemento, che si ripetono in modo simile al crescere del numero atomico Z. Pertanto, a diversi numeri atomici (ossia ad elementi diversi ordinati per massa) corrispondono diverse proprietà chimiche macroscopiche, che si ripetono periodicamente in modo simile per configurazioni elettroniche che hanno una stabilità energetica comparabile, e questo accade per analoghi gradi di riempimento dell'orbitale, che si ripetono con periodo variabile perché variabile è il massimo riempimento dei vari orbitali.
La forma corretta della tavola periodica degli elementi fu pertanto inizialmente determinata solo da osservazioni macroscopiche, senza la presenza di un modello microscopico a cui fare riferimento. Successivamente questa forma è stata "confermata" con la scoperta della struttura microscopica degli atomi e quindi delle loro modalità di interazione.
Variazione periodica [modifica]
Le varie caratteristiche degli elementi chimici che variano periodicamente (indicate nell'elenco precedentemente) sono utilizzate per categorizzare l'elemento stesso (come ad esempio il gruppo di appartenenza).
Più precisamente, il
raggio atomico aumenta nello stesso gruppo se ci spostiamo verso gli elementi in basso e diminuisce se avanziamo da sinistra a destra nello stesso periodo; questo è dovuto al fatto che scendendo nel gruppo il
numero quantico principale n aumenta e ciò fa sì che l'atomo abbia una
nuvola elettronica più sviluppata, mentre andando da sinistra a destra nel periodo
n rimane uguale, mentre varia il numero di protoni all'interno del nucleo, facendo aumentare le forze nucleari di attrazione tra gli elettroni e il nucleo attorno al quale gravitano, con la conseguente diminuzione del raggio atomico.
Sia
l'energia di ionizzazione, l'
elettronegatività che l'
affinità elettronica diminuiscono scendendo in un gruppo ed aumentano avanzando da sinistra verso destra nel periodo. Questo è dovuto al fatto che scendendo nel gruppo gli elettroni nell'ultimo livello energetico sono attirati sempre con meno forza per diminuzione delle forze nucleari (gli atomi sono meno elettronegativi) e questo fa diminuire l'energia necessaria per strapparli (diminuisce l'energia di ionizzazione) e l'energia liberata quando l'atomo acquista un elettrone (affinità elettronica). Andando da sinistra verso destra in un periodo invece gli elettroni saranno attirati sempre con maggior forza dalle forze nucleari (aumenta l'elettronegatività) e questo fa aumentare l'energia per strappargli un elettrone (aumenta l'energia di ionizzazione) e l'energia liberata per acquisto di un elettrone (affinità elettronica). Secondo la teoria di Niels Bohr, in cui il numero di elettroni aumenta con l'aumentare del numero degli orbitali (k=2×1²=2; l=2×2²=8; m=2×3²=18), anche la forma della tavola dovrebbe cambiare. Questa teoria porrebbe fine anche al problema della collocazione delle terre rare. Bisogna prendere il Z dei gas nobili che è:
2, 10, 18, 36, 54, 86, 118.
Occorre fare la differenza tra due gas adiacenti per trovare il numero degli elementi contenuti nel proprio periodo:
10-2=8; 18-10=8; 36-18=18; 54-36=18; 86-54=32; 118-86=32
Si noti che il risultato è identico al risultato delle moltiplicazioni sopra scritte e che si ripete 2 volte prima di cambiare.
In questo modo si capisce il perché dei "salti di due caselle": dopo l'elio si salta, poi ci sono due periodi che combaciano (2 e 3), poi ci sono i metalli di transizione (4 e 5), le terre rare (6 e 7). In tal modo si può anche scoprire il Z del prossimo gas nobile, 118+(2×5²)= 168.
Rappresentazioni alternative della tavola periodica [modifica]
Tavola periodica "a spirale" di Jan Scholten
Tavola periodica "a spirale" di Theodor Benfey (1960)
Tavola periodica "circolare"
Tavola periodica nel formato "TROPE" (The Ring Of Periodic Elements)
Tavola periodica "a fiore"
Tavola periodica "a piramide"
Tavola periodica nel formato "Stowe"
Tavola periodica nel formato "Tarantola"
Tavola periodica nel formato "Zmaczynski & Bayley"
Tavola periodica nel formato "ADOMAH" (V.Tsimmerman)
- ^ Manuela Campanelli. Due nuovi elementi nella Tavola periodica: flerovio e livermorio. corriere.it, 20 dicembre 2011. URL consultato in data 10 gennaio 2012.
- ^ Silvestroni, op. cit., p. 29
- ^ a b Greenwood, Norman N., Earnshaw A., Chemistry of the Elements, Oxford, Pergamon, 1984, 24–27. ISBN 0-08-022057-6
- ^ a b Cronyn, Marshall W. (agosto 2003). The Proper Place for Hydrogen in the Periodic Table. Journal of Chemical Education 80 (8): 947–951. DOI:10.1021/ed080p947. Bibcode 2003JChEd..80..947C.
- ^ a b Gray, p. 12
- ^ Samanta, C., Chowdhury, P. Roy, Basu, D. N. (2007). Predictions of alpha decay half lives of heavy and superheavy elements. Nucl. Phys. A 789: 142–154. DOI:10.1016/j.nuclphysa.2007.04.001. Bibcode 2007NuPhA.789..142S.
- ^ a b Leigh G. J., Nomenclature of Inorganic Chemistry: Recommendations 1990, Blackwell Science, 1990. ISBN 0-632-02494-1
- ^ Leigh Jeffery. Periodic Tables and IUPAC. Chemistry International: The News Magazine of The International Union of Pure and Applied Chemistry (IUPAC). URL consultato in data 23 marzo 2011.
- ^ Scerri E. R., The Periodic Table: Its Story and its Significance, Oxford University Press. ISBN 978-0-19-530573-9
- ^ a b Moore, p. 111
- ^ Stephen H. Stoker, General, organic, and biological chemistry, New York, Houghton Mifflin, 2007. ISBN 978-0-618-73063-6. OCLC 52445586
- ^ Joseph Mascetta, Chemistry The Easy Way, 4a ed., New York, Hauppauge, 2003. ISBN 978-0-7641-1978-1. OCLC 52047235
- ^ John Kotz, Paul Treichel, John Townsend, Chemistry and Chemical Reactivity, 7a ed., Belmont, Thomson Brooks/Cole, 2009, Vol. 2. ISBN 978-0-495-38712-1. OCLC 220756597
- ^ Chris Jones, d- and f-block chemistry, New York, J. Wiley & Sons, 2002. ISBN 978-0-471-22476-1. OCLC 300468713
- ^ Gimigliano, op. cit., p. 158
- ^ IUPAC Periodic Table
- ^ IUPAC Periodic Table 2007 .pdf
- ^ Silvestroni, op. cit., pp. 25-29
- Paolo Silvestroni, Fondamenti di chimica, 10a ed., CEA, 1996. ISBN 88-408-0998-8
- Antonio F. Gimigliano, Chimica per le scuole medie superiori, Giunti Marzocco, 1991. ISBN 88-09-60519-5
- R. Barbucci, A. Sabatini, P. Dapporto, Tavola periodica e proprietà degli elementi, Firenze, Edizioni V. Morelli, 1998. ISBN 88-1020-000-0
- Francesco Borgese, Gli elementi della tavola periodica. Rinvenimento, proprietà, usi. Prontuario chimico, fisico, geologico, Roma, CISU, 1993. ISBN 88-7975-077-1
- Philip Ball, The Ingredients: A Guided Tour of the Elements, Oxford University Press, 2002. ISBN 0-19-284100-9
- J. Bouma (1989). An Application-Oriented Periodic Table of the Elements. J. Chem. Ed. 66 (9). DOI:10.1021/ed066p741. Bibcode 1989JChEd..66..741B.
- Theodore Gray, The Elements: A Visual Exploration of Every Known Atom in the Universe, New York, Black Dog & Leventhal Publishers, 2009. ISBN 978-1-57912-814-2
- Hjørland Birger (2011). The periodic table and the philosophy of classification. Knowledge Organization 38 (1).
- Sam Kean, The Disappearing Spoon - and other true tales from the Periodic Table, Londra, Black Swan, 2010. ISBN 978-0-552-77750-6
- Primo Levi, The Periodic Table [1975], Londra, Penguin Books, 1984. ISBN 978-0-14-139944-7
- E. G. Mazurs, Graphical Representations of the Periodic System During One Hundred Years, Alabama, University of Alabama Press, 1974.
- John Moore, Chemistry For Dummies, New York, Wiley Publications, 2003. ISBN 978-0-7645-5430-8
- Eric Scerri, The periodic table: its story and its significance, Oxford, Oxford University Press, 2007. ISBN 0-19-530573-6
- (WIKIPEDIA.IT)